- La Asociación Internacional para el Estudio del Dolor (IASP) definió el dolor neuropático como "dolor iniciado o causado por una lesión primaria o disfunción del sistema nervioso"
- Posteriormente, The Special Interest Group on Neuropathic Pain (NeuPSIG) lo redefinió como "dolor que surge como consecuencia directa de una lesión o enfermedad que afecta al sistema somatosensorial".
- Expresión de plasticidad maladaptativa del sistema nervioso que produce una serie de cambios que constituyen un estado de "enfermedad neuronal".
Según van Hecke (4), la prevalencia estimada de dolor con características neuropáticas en la población general está entre el 6,9 y 10%.
¿Cómo se manifiesta el dolor neuropático?
- Dolor espontáneo, continuo o intermitente.
- Puede ser quemante, paroxístico, como de descargas eléctricas, o como un dolor provocado.
- Síntomas autonómicos: sudoración, enrojecimiento, tumefacción.
- Alteraciones sensoriales, signos negativos: cuando existe un daño nervioso, disminuye la aferencia sensorial de los estímulos sensitivos.
- Alteraciones sensoriales, signos positivos: Disestesia, alodinia, hiperalgesia, hiperpatía, hipersensibilidad localizada.
- Alteraciones del sueño: suelen acompañar la sintomatología dolorosa.
"Clasificación" del dolor:

- van Hecke et al (4), en su revisión sistemática, clasifican el dolor neuropático en dos grandes grupos:
1. Dolor crónico con características neuropáticas.
2. Dolor neuropático asociado a condiciones concretas (neuralgia postherpética, neuralgia del trigémino, neuropatía periférica asociada a diabetes, neuralgia glosofaríngea...)
Esta clasificación es interesante a la hora de distinguir a grandes rasgos los tipos de dolor neuropático, teniendo como finalidad el estudio y la investigación para la mejora del tratamiento del dolor.
- Costigan et al (1) realizan otra clasificación más detallada:
1. Dolor nociceptivo: en concordancia con la teoría de especificidad de la que se habla más adelante, se define como una sensación desagradable (lo suficiente como para no ser ignorada) que se transmite a través de vías nociceptivas especializadas. Ocurre sólo como respuesta a un estímulo doloroso y cesa cuando éste se detiene, es decir, no se mantiene en el tiempo una vez el estímulo desaparece.
2. Dolor inflamatorio: en este caso no sólo hay estímulo doloroso sino que ya se produce un daño tisular, con su consecuente respuesta inflamatoria. Así, para ayudar a proteger y reparar la zona dañada, los estímulos que habitualmente no producen dolor, ahora lo producen.
Esta modificación en el umbral de dolor, que ahora es más bajo, sucede en el área de la inflamación y en la contigua, debido a la plasticidad de los nociceptores y las vías centrales.
Lo normal es que el dolor inflamatorio desaparezca una vez resuelto el daño del tejido, aunque puede prolongarse durante un tiempo.
3. Dolor disfuncional: se habla de un dolor que no es adaptativo, es decir, que ni protege ni apoya la reparación tisular, sino que está causado por un mal funcionamiento del sistema somatosensorial.
4. Dolor neuropático: en este caso, la pérdida de función y el dolor están íntimamente relacionados. Se trata de una reacción del sistema nervioso a un daño neural.
Se distingue entre dolor neuropático periférico (a partir de lesiones del sistema nervioso periférico, como los causados por traumatismos, enfermedades metabólicas, infecciones, etc.) y el dolor neuropático central (lesión medular, ACV, esclerosis múltiple...). Se conocen también como síndromes neuropáticos el Síndrome de Dolor Regional Complejo y el Dolor de Miembro Fantasma.
Tanto el dolor disfuncional como el neuropático tienen en común los siguientes aspectos:
- Sumación temporal progresiva en respuesta a un estímulo repetido.
- Extensión espacial.
- Disminución del umbral del dolor.
Teorías sobre el dolor:
Según Cerveró (2) Existen, a grandes rasgos, dos teorías sobre los mecanismos de dolor anormal, que en algunos aspectos se contradicen.
- Especificidad: habla del dolor como resultado de una secuencia de cadenas neuronales nociceptivas. Sin embargo, no explica los patrones anormales en receptores de bajo umbral.
- Patrones de neuronas y sistemas sensoriales inespecíficos: esta teoría niega la esta existencia de cadenas neuronales específicas del dolor (es decir, contradice a la anterior), sino que habla de patrones espacio temporales de impulsos nerviosos en sistemas que no son específicos de la nocicepción. Esta teoría tiene el inconveniente de que existe evidencia de la existencia de nociceptores específicos tanto en sistema nervioso central como periférico.
Se habla entonces de que descargas nociceptivas prolongadas pueden alterar el equilibrio existente entre el dolor normal o nociceptivo y los sistemas sensoriales, de manera que se producen sensaciones evocadas con variación en intensidad y duración. Si estas alteraciones son temporales, el sistema nervioso tiende a poder restaurar dicho equilibrio, pero si se prolongan en el tiempo o son muy intensas, pueden provocar cambios a nivel neurológico, perdiéndose la relación entre lesión y dolor.
Según Nielsen et al (2008), Staud et al (2008) y Julien et al (2005), el dolor disfuncional puede deberse en algunos casos a una amplificación de la información nociceptiva, con un equilibrio alterado entre excitación e inhibición en los circuitos del sistema nervioso central (1).
En el caso del dolor neuropático, la causa principal y el daño nervioso inician una cascada de cambios por una plasticidad "maladaptativa", que producen y mantienen dicho dolor.
- Nuevos analgésicos: enlace revista Investigación y ciencia.
- Posteriormente, The Special Interest Group on Neuropathic Pain (NeuPSIG) lo redefinió como "dolor que surge como consecuencia directa de una lesión o enfermedad que afecta al sistema somatosensorial".
- Expresión de plasticidad maladaptativa del sistema nervioso que produce una serie de cambios que constituyen un estado de "enfermedad neuronal".
Según van Hecke (4), la prevalencia estimada de dolor con características neuropáticas en la población general está entre el 6,9 y 10%.
- Dolor espontáneo, continuo o intermitente.
- Puede ser quemante, paroxístico, como de descargas eléctricas, o como un dolor provocado.
- Síntomas autonómicos: sudoración, enrojecimiento, tumefacción.
- Alteraciones sensoriales, signos negativos: cuando existe un daño nervioso, disminuye la aferencia sensorial de los estímulos sensitivos.
- Alteraciones sensoriales, signos positivos: Disestesia, alodinia, hiperalgesia, hiperpatía, hipersensibilidad localizada.
- Alteraciones del sueño: suelen acompañar la sintomatología dolorosa.
Hiperpatía
|
Aumento de la respuesta al estímulo
doloroso
|
Disestesias
|
Sensación dolorosa en ausencia de
estímulo (quemante, eléctrica, cuchillada, ardor)
|
Hiperalgesia
|
Incremento de la percepción en la
intensidad del impulso doloroso
|
Hipoestesia
|
Reducción de la sensibilidad al
tacto
|
Alodinia
|
Dolor inducido por un estímulo no
doloroso (contacto con la ropa, por ejemplo)
|
Radiculalgia
|
Dolor a lo largo de la distribución de
una o varias raíces sensitivas
|
“Trigger point” o punto gatillo
|
Área de hipersensibilidad situada en el
músculo o tejido conectivo
|
Tabla I. Definiciones de términos utilizados habitualmente
en el campo del dolor neuropático. Según Cruciani y Nieto(5) y los expertos de la Cátedra Extraordinaria del Dolor de la Univeridad de Salamanca (11).
"Clasificación" del dolor:

- van Hecke et al (4), en su revisión sistemática, clasifican el dolor neuropático en dos grandes grupos:
1. Dolor crónico con características neuropáticas.
2. Dolor neuropático asociado a condiciones concretas (neuralgia postherpética, neuralgia del trigémino, neuropatía periférica asociada a diabetes, neuralgia glosofaríngea...)
Esta clasificación es interesante a la hora de distinguir a grandes rasgos los tipos de dolor neuropático, teniendo como finalidad el estudio y la investigación para la mejora del tratamiento del dolor.
- Costigan et al (1) realizan otra clasificación más detallada:
1. Dolor nociceptivo: en concordancia con la teoría de especificidad de la que se habla más adelante, se define como una sensación desagradable (lo suficiente como para no ser ignorada) que se transmite a través de vías nociceptivas especializadas. Ocurre sólo como respuesta a un estímulo doloroso y cesa cuando éste se detiene, es decir, no se mantiene en el tiempo una vez el estímulo desaparece.
2. Dolor inflamatorio: en este caso no sólo hay estímulo doloroso sino que ya se produce un daño tisular, con su consecuente respuesta inflamatoria. Así, para ayudar a proteger y reparar la zona dañada, los estímulos que habitualmente no producen dolor, ahora lo producen.
Esta modificación en el umbral de dolor, que ahora es más bajo, sucede en el área de la inflamación y en la contigua, debido a la plasticidad de los nociceptores y las vías centrales.
Lo normal es que el dolor inflamatorio desaparezca una vez resuelto el daño del tejido, aunque puede prolongarse durante un tiempo.
3. Dolor disfuncional: se habla de un dolor que no es adaptativo, es decir, que ni protege ni apoya la reparación tisular, sino que está causado por un mal funcionamiento del sistema somatosensorial.
4. Dolor neuropático: en este caso, la pérdida de función y el dolor están íntimamente relacionados. Se trata de una reacción del sistema nervioso a un daño neural.
Se distingue entre dolor neuropático periférico (a partir de lesiones del sistema nervioso periférico, como los causados por traumatismos, enfermedades metabólicas, infecciones, etc.) y el dolor neuropático central (lesión medular, ACV, esclerosis múltiple...). Se conocen también como síndromes neuropáticos el Síndrome de Dolor Regional Complejo y el Dolor de Miembro Fantasma.
Tanto el dolor disfuncional como el neuropático tienen en común los siguientes aspectos:
- Sumación temporal progresiva en respuesta a un estímulo repetido.
- Extensión espacial.
- Disminución del umbral del dolor.
Teorías sobre el dolor:
Según Cerveró (2) Existen, a grandes rasgos, dos teorías sobre los mecanismos de dolor anormal, que en algunos aspectos se contradicen.
- Especificidad: habla del dolor como resultado de una secuencia de cadenas neuronales nociceptivas. Sin embargo, no explica los patrones anormales en receptores de bajo umbral.
- Patrones de neuronas y sistemas sensoriales inespecíficos: esta teoría niega la esta existencia de cadenas neuronales específicas del dolor (es decir, contradice a la anterior), sino que habla de patrones espacio temporales de impulsos nerviosos en sistemas que no son específicos de la nocicepción. Esta teoría tiene el inconveniente de que existe evidencia de la existencia de nociceptores específicos tanto en sistema nervioso central como periférico.
Se habla entonces de que descargas nociceptivas prolongadas pueden alterar el equilibrio existente entre el dolor normal o nociceptivo y los sistemas sensoriales, de manera que se producen sensaciones evocadas con variación en intensidad y duración. Si estas alteraciones son temporales, el sistema nervioso tiende a poder restaurar dicho equilibrio, pero si se prolongan en el tiempo o son muy intensas, pueden provocar cambios a nivel neurológico, perdiéndose la relación entre lesión y dolor.
Según Nielsen et al (2008), Staud et al (2008) y Julien et al (2005), el dolor disfuncional puede deberse en algunos casos a una amplificación de la información nociceptiva, con un equilibrio alterado entre excitación e inhibición en los circuitos del sistema nervioso central (1).
En el caso del dolor neuropático, la causa principal y el daño nervioso inician una cascada de cambios por una plasticidad "maladaptativa", que producen y mantienen dicho dolor.
Mecanismos neurofisiológicos del dolor:
Los mecanismos son distintos en función del tipo de dolor. Es decir, el dolor "normal" o nociceptivo, y el dolor anormal (comúnmente denominado neuropático, aunque también se le dan otros nombres según la etiología o las características), son dos extremos, comprendiendo entre ambos una gran variedad de sensaciones que integra el sistema nervioso central. Sin embargo, existen también mecanismos comunes.
 Mecanismos comunes en diferentes estados de dolor crónico:
Mecanismos comunes en diferentes estados de dolor crónico:
- Mediadores de detección inmune: después de un daño del tejido nervioso, las células inmunitarias periféricas y la microglía de la médula espinal producen mediadores inflamatorios y contribuyen a la activación neuronal .
- Sensibilización periférica: la excitabilidad de la membrana de las células nociceptoras aumenta a causa de la inflamación y la activación de las vías del dolor.
- Centralización (1, 5): es un mecanismo patofisiológico común al dolor inflamatorio, neuropático y disfuncional. La actividad generada por los nociceptores durante la inflamación conllevan cambios en el asta posterior de la médula (excitabilidad de las neuronas sensoriales dañadas). Esto produce una amplificación de las entradas sensoriales. Además, se producen alteraciones en la liberación de neurotransmisores (moduladores y excitadores), cambios degenerativos sensoriales primarios, desinhibición neuronal y reorganización sináptica. En el caso del dolor neuropático, el desencadenante de la sensibilización central es la actividad de los nociceptores en los nervios lesionados, que alteran las vías aferentes en la médula espinal.
Mecanismos generadores de dolor neuropático:
Incluso habiendo desaparecido la causa original del daño al tejido nervioso, este síndrome de hipersensibilidad puede prolongarse. Aún así, el dolor neuropático no es una consecuencia inevitable en lesiones neurológicas, sino que existen factores o riesgos asociados:
- Madurez del sistema nervioso: por ejemplo, la avulsión del plexo braquial en adultos desarrolla dolor neuropático un 40% más que en la obstétrica).
- Género, edad.
- Zona anatómica de la lesión.
- Severidad del dolor agudo postoperatorio.
Se producen dos procesos interdependientes en el desarrollo del dolor neuropático:
- Alteración del equilibrio entre reacciones compensatorias y descompensatorias del sistema nervioso al daño neural.
- Antecedentes genéticos que pueden proteger a las persona del establecimiento del dolor neuropático.
Aunque muchos de los cambios que se producen son potencialmente buenos o adaptativos, otros son claramente desencadenantes (justo después del del daño inicial) o factores que mantienen el dolor (se desarrollan más tarde).
- Generación de impulsos ectópicos: la actividad ectópica puede generarse en cualquier nivel anatómico proximal a las regiones cerebrales que median los procesos sensoriales (1)
- Transducción ectópica: la sensibilidad aumentada de neuronas sensitivas dañadas pueden originar dolor espontáneo.
- Centralización: la facilitación sináptica contrivuye a la alodinia dinámica tactil también como hipersensibilidad secundaria. Además, aunque la sensibilización central ha sido descrita como un proceso en el asta posterior, también se dan alteraciones sinápticas similares en estructuras implicadas en aspectos emocionales del dolor (como la amígdala, lla circunvolución del cíngulo, y la corteza prefrontal).
Tratamiento:
Por desgracia, no existe un tratamiento completamente efectivo para el dolor neuropático. Sin embargo, existen varias opciones que pueden paliar o mejorar este síndrome.
1. Tratamiento farmacológico:
- Anticonvulsivantes: como la Gabapentina, lamotrigina y la preglabalina. La combinación de gabapentina y morfina parece más eficaz, según estudios recientes. (5). En casos en los que estos fármacos no funcionan, se prueba con Oxcarbazepina, levetiracetam, topiramato, zonisanida y tiagabina.
- Antidepresivos.
- Anestésicos locales.
- Opiáceos.
- Antagonistas de los receptores NMDA.
- Antagonistas opiáceos.
- Cannabinoides: utilizado especialmente en Esclerosis Múltiple, pero también en Lesión Medular, , lesiones del Plexo Braquial, Dolor de Miembro Fantasma...
A continuación se presentan unas tablas de actuación farmacológica, según un artículo de González- Escalada (12)
2. Tratamiento rehabilitador o conservador:
- Mirror Therapy o Terapia de Neuronas Espejo: en el caso del dolor neuropático, se basa en la suposición de que la plasticidad neuronal puede corregir las alteraciones centrales de percepción del dolor "engañando" al cerebro con la percepción visual: la ilusión visual del movimiento de la extremidad afectada crea una retroalimentación a la corteza motora e interrumpe el dolor. A través de un espejo, al mover el miembro sano, se simula el movimiento del miembro doloroso.
- Visualización. Se basa en que la asociación entre visión y acción implica efectos moduladores a nivel del sistema nervioso central. La percepción del movimiento no necesita de hecho ver la acción en sí. La vivencia inducida del movimiento puede conseguir que, a nivel central, se prediga el movimiento y sus consecuencias aunque no se haya realizado la acción sino sólo visualizada o inducida por otros componentes sensoriales.
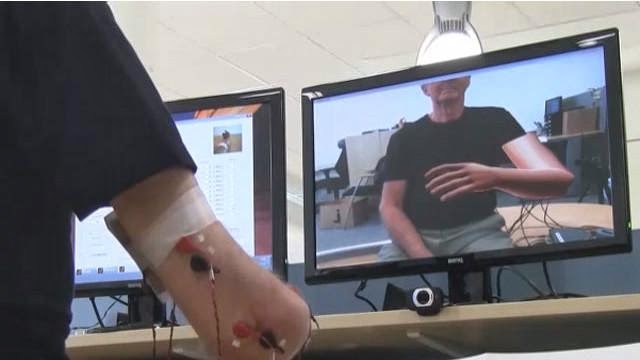 - Feedback a través de realidad virtual o realidad aumentada: a través de una extremidad virtual, se simula el movimiento que se le pide al paciente que haga con el miembro afectado (por ejemplo el que haría con la mano aunque ésta haya sido amputada). El efecto de la neuroplasticidad y la comunicación entre ambos hemisferios es diferente entre la práctica de la ejecución motriz y la imaginación del movimiento, lo que sugiere que el control voluntario del movimiento o de la creación voluntaria del movimiento puede llegar a reducir el dolor neuropático.
- Feedback a través de realidad virtual o realidad aumentada: a través de una extremidad virtual, se simula el movimiento que se le pide al paciente que haga con el miembro afectado (por ejemplo el que haría con la mano aunque ésta haya sido amputada). El efecto de la neuroplasticidad y la comunicación entre ambos hemisferios es diferente entre la práctica de la ejecución motriz y la imaginación del movimiento, lo que sugiere que el control voluntario del movimiento o de la creación voluntaria del movimiento puede llegar a reducir el dolor neuropático.
Estudios recientes demuestran que estas técnicas son efectivas para el tratamiento de dolores neuropáticos de tipo SDRC o de miembro fantasma.
3. Tratamiento quirúrgico: en dolor de miembro fantasma, se contempla la posibilidad de este tipo de intervención en casos de remodelamiento del muñón, reamputación proximal o por existencia de neurioma (11)
4. Otros tratamientos e investigación en proceso de experimentación:
- Estimulación magnética transcraneal: es una forma de estimulación eléctrica no invasiva, sin electrodos, por inducción electromagnética (14) para la neuromodulación de redes neuronales específicas. A baja frecuencia, parece que no tiene efectos signiticativos; a alta frecuencia, presenta efectos positivos a corto plazo (15).
- Estimulación craneal mediante electroterapia: de momento no se han encontrado diferencias signiticativas con la estimulación simulada (15). Parece ser que es está llevando a cabo un estudio en el Hospital Nacional de Parapléjicos de Toledo, aunque no tengo datos disponibles.
- Estimulación eléctrica medular: en casos de Síndrome Regional Complejo (SDRC) en los que el tratamiento conservador no haya obtenido resultado. (11)
- Bloqueos nerviosos:bloqueo nervioso simpático en SDRC, como el bloqueo simpático regional. bloqueo epidural continuo y el bloqueo del ganglio estrellado. (11)
- Simpatectomía a través de radioterapia, también en SDRC.
- Déficit congénito de receptores ldl: abordaje mediante trasplante celular combinado. Investigadora principal: Paloma Maganto Suárez. Hospital Puerta de Hierro.
- Estudio multicéntrico de validez y fiabilidad de la Escala de Conductas Indicadoras de Dolor para medir el dolor en pacientes críticos, no comunicativos y sometidos a ventilación mecánica. Investigador principal: Ignacio Latorre Marco. Hospital Puerta de Hierro.
- “Modulación de la neugenesis endógena por la administración de células madre mesenquimales en lesiones traumáticas del sistema nervioso”. Investigador principal: Jesús Vaquero Crespo. Hospital Puerta de Hierro.
- Ensayo clínico comparativo de QUTENZA™ frente a pregabalina, tratamiento de primera línea frente al dolor neuropático periférico. Investigadora principal: Maija Haanpää. Hospital Universitario de Helsinki.
Los mecanismos son distintos en función del tipo de dolor. Es decir, el dolor "normal" o nociceptivo, y el dolor anormal (comúnmente denominado neuropático, aunque también se le dan otros nombres según la etiología o las características), son dos extremos, comprendiendo entre ambos una gran variedad de sensaciones que integra el sistema nervioso central. Sin embargo, existen también mecanismos comunes.
 Mecanismos comunes en diferentes estados de dolor crónico:
Mecanismos comunes en diferentes estados de dolor crónico:- Mediadores de detección inmune: después de un daño del tejido nervioso, las células inmunitarias periféricas y la microglía de la médula espinal producen mediadores inflamatorios y contribuyen a la activación neuronal .
- Sensibilización periférica: la excitabilidad de la membrana de las células nociceptoras aumenta a causa de la inflamación y la activación de las vías del dolor.
- Centralización (1, 5): es un mecanismo patofisiológico común al dolor inflamatorio, neuropático y disfuncional. La actividad generada por los nociceptores durante la inflamación conllevan cambios en el asta posterior de la médula (excitabilidad de las neuronas sensoriales dañadas). Esto produce una amplificación de las entradas sensoriales. Además, se producen alteraciones en la liberación de neurotransmisores (moduladores y excitadores), cambios degenerativos sensoriales primarios, desinhibición neuronal y reorganización sináptica. En el caso del dolor neuropático, el desencadenante de la sensibilización central es la actividad de los nociceptores en los nervios lesionados, que alteran las vías aferentes en la médula espinal.
Mecanismos generadores de dolor neuropático:
Incluso habiendo desaparecido la causa original del daño al tejido nervioso, este síndrome de hipersensibilidad puede prolongarse. Aún así, el dolor neuropático no es una consecuencia inevitable en lesiones neurológicas, sino que existen factores o riesgos asociados:
- Madurez del sistema nervioso: por ejemplo, la avulsión del plexo braquial en adultos desarrolla dolor neuropático un 40% más que en la obstétrica).
- Género, edad.
- Zona anatómica de la lesión.
- Severidad del dolor agudo postoperatorio.
Se producen dos procesos interdependientes en el desarrollo del dolor neuropático:
- Alteración del equilibrio entre reacciones compensatorias y descompensatorias del sistema nervioso al daño neural.
- Antecedentes genéticos que pueden proteger a las persona del establecimiento del dolor neuropático.
Aunque muchos de los cambios que se producen son potencialmente buenos o adaptativos, otros son claramente desencadenantes (justo después del del daño inicial) o factores que mantienen el dolor (se desarrollan más tarde).
- Generación de impulsos ectópicos: la actividad ectópica puede generarse en cualquier nivel anatómico proximal a las regiones cerebrales que median los procesos sensoriales (1)
- Transducción ectópica: la sensibilidad aumentada de neuronas sensitivas dañadas pueden originar dolor espontáneo.
- Centralización: la facilitación sináptica contrivuye a la alodinia dinámica tactil también como hipersensibilidad secundaria. Además, aunque la sensibilización central ha sido descrita como un proceso en el asta posterior, también se dan alteraciones sinápticas similares en estructuras implicadas en aspectos emocionales del dolor (como la amígdala, lla circunvolución del cíngulo, y la corteza prefrontal).
Tratamiento:
Por desgracia, no existe un tratamiento completamente efectivo para el dolor neuropático. Sin embargo, existen varias opciones que pueden paliar o mejorar este síndrome.
1. Tratamiento farmacológico:
- Anticonvulsivantes: como la Gabapentina, lamotrigina y la preglabalina. La combinación de gabapentina y morfina parece más eficaz, según estudios recientes. (5). En casos en los que estos fármacos no funcionan, se prueba con Oxcarbazepina, levetiracetam, topiramato, zonisanida y tiagabina.
- Antidepresivos.
- Anestésicos locales.
- Opiáceos.
- Antagonistas de los receptores NMDA.
- Antagonistas opiáceos.
- Cannabinoides: utilizado especialmente en Esclerosis Múltiple, pero también en Lesión Medular, , lesiones del Plexo Braquial, Dolor de Miembro Fantasma...
A continuación se presentan unas tablas de actuación farmacológica, según un artículo de González- Escalada (12)
2. Tratamiento rehabilitador o conservador:
- Mirror Therapy o Terapia de Neuronas Espejo: en el caso del dolor neuropático, se basa en la suposición de que la plasticidad neuronal puede corregir las alteraciones centrales de percepción del dolor "engañando" al cerebro con la percepción visual: la ilusión visual del movimiento de la extremidad afectada crea una retroalimentación a la corteza motora e interrumpe el dolor. A través de un espejo, al mover el miembro sano, se simula el movimiento del miembro doloroso.
- Visualización. Se basa en que la asociación entre visión y acción implica efectos moduladores a nivel del sistema nervioso central. La percepción del movimiento no necesita de hecho ver la acción en sí. La vivencia inducida del movimiento puede conseguir que, a nivel central, se prediga el movimiento y sus consecuencias aunque no se haya realizado la acción sino sólo visualizada o inducida por otros componentes sensoriales.
 - Feedback a través de realidad virtual o realidad aumentada: a través de una extremidad virtual, se simula el movimiento que se le pide al paciente que haga con el miembro afectado (por ejemplo el que haría con la mano aunque ésta haya sido amputada). El efecto de la neuroplasticidad y la comunicación entre ambos hemisferios es diferente entre la práctica de la ejecución motriz y la imaginación del movimiento, lo que sugiere que el control voluntario del movimiento o de la creación voluntaria del movimiento puede llegar a reducir el dolor neuropático.
- Feedback a través de realidad virtual o realidad aumentada: a través de una extremidad virtual, se simula el movimiento que se le pide al paciente que haga con el miembro afectado (por ejemplo el que haría con la mano aunque ésta haya sido amputada). El efecto de la neuroplasticidad y la comunicación entre ambos hemisferios es diferente entre la práctica de la ejecución motriz y la imaginación del movimiento, lo que sugiere que el control voluntario del movimiento o de la creación voluntaria del movimiento puede llegar a reducir el dolor neuropático.Estudios recientes demuestran que estas técnicas son efectivas para el tratamiento de dolores neuropáticos de tipo SDRC o de miembro fantasma.
3. Tratamiento quirúrgico: en dolor de miembro fantasma, se contempla la posibilidad de este tipo de intervención en casos de remodelamiento del muñón, reamputación proximal o por existencia de neurioma (11)
4. Otros tratamientos e investigación en proceso de experimentación:
- Estimulación magnética transcraneal: es una forma de estimulación eléctrica no invasiva, sin electrodos, por inducción electromagnética (14) para la neuromodulación de redes neuronales específicas. A baja frecuencia, parece que no tiene efectos signiticativos; a alta frecuencia, presenta efectos positivos a corto plazo (15).
- Estimulación craneal mediante electroterapia: de momento no se han encontrado diferencias signiticativas con la estimulación simulada (15). Parece ser que es está llevando a cabo un estudio en el Hospital Nacional de Parapléjicos de Toledo, aunque no tengo datos disponibles.
- Estimulación eléctrica medular: en casos de Síndrome Regional Complejo (SDRC) en los que el tratamiento conservador no haya obtenido resultado. (11)
- Bloqueos nerviosos:bloqueo nervioso simpático en SDRC, como el bloqueo simpático regional. bloqueo epidural continuo y el bloqueo del ganglio estrellado. (11)
- Simpatectomía a través de radioterapia, también en SDRC.
- Déficit congénito de receptores ldl: abordaje mediante trasplante celular combinado. Investigadora principal: Paloma Maganto Suárez. Hospital Puerta de Hierro.
- Estudio multicéntrico de validez y fiabilidad de la Escala de Conductas Indicadoras de Dolor para medir el dolor en pacientes críticos, no comunicativos y sometidos a ventilación mecánica. Investigador principal: Ignacio Latorre Marco. Hospital Puerta de Hierro.
- “Modulación de la neugenesis endógena por la administración de células madre mesenquimales en lesiones traumáticas del sistema nervioso”. Investigador principal: Jesús Vaquero Crespo. Hospital Puerta de Hierro.
- Ensayo clínico comparativo de QUTENZA™ frente a pregabalina, tratamiento de primera línea frente al dolor neuropático periférico. Investigadora principal: Maija Haanpää. Hospital Universitario de Helsinki.
- Nuevos analgésicos: enlace revista Investigación y ciencia.
Algunos estudios recientes sobre el tema:
1. Dolor neuropático: una respuesta maladaptativa al daño del sistema nervioso.
Costigan M, Scholz J, Woolf CJ: Neuropathic pain: a maladaptative response of the nervous system to damage. Annu Rev Nueurosci 2009; 32: 1-32.
2. Neurobiología del dolor. Cerveró, F: Neurobiología del dolor. Rev Neurol 2000; 30 (6) 551-555.
3. Eficacia del levetiracetam en el tratamiento del dolor neuropático.
Del Pozo E, Pereira- Pérez E, González- Contreras LG: Eficacia del levetiracetam en el tratamiento del dolor neuropático. Rev Neurol 2011; 53 (2): 65-72.
Se trata de una revisión bibliográfica, y para resumir un poco, la conclusión es que no hay demasiada evidencia científica sobre la eficacia del levetiraceram en comparación con el placebo.
4. Revisión sistemática de dolor neuropático: van Hecke O, Austin SK, Khan RA, Smith BH, Torrance N: Neuropathic pain in the general population: A systematic review of epidemiological studies. Pain 2013; 155 (4): 654-662.
5. Fisiopatología y tratamiento del dolor neuropático: Cruciani RA, Nieto MJ: Fisiopatología y tratamiento del dolor neuropático. Rev. Soc. Esp. Dolor 2006; 5: 312-327.
La conclusión es que no hay evidencia de que el tratamiento funcione, aunque no se produjeron efectos secundarios.
7. Tratamiento del dolor neuropático con lacosamida
8. Ziconotide: una alternativa innovadora en el tratamiento del dolor neuropático intenso.
9. Realidad aumentada en tratamiento del dolor de miembro fantasma: Ortiz- Catalán et al: Treatment os phantom limb pain (PLP) based on augmented reality gaming controlled by myoelectric pattern recognition: a case study of a chronic PLP patient. Frontiers of Neuroscience 2014; 24 (8): 1-6.
10. "Kinestesia":Dieter KC et al: Kinesthesis can make an invisible hand visible. Psychological Science 2014; 25 (1) 66-75.
11. Reunión de Expertos en Dolor neuropático. Cátedra Extraordinaria del Dolor
"Fundación Grünenthal" de la Universidad de Salamanca.
12. Cannabis y Cannabinoides en el tratamiento del dolor neuropático. Durán M, Capellá D: Cannabis y Cannabinoides en el tratamiento del dolor neuropático. DOLOR 2000; 20.
13. Recomendaciones para el tratamiento del dolor neuropático. González - Escalada, JR et al.: Recomendaciones para el tratamiento del dolor neuropático. Rev. Soc. Esp. Dolor[online]. 2009; 16 (8) 445-467.
11. Reunión de Expertos en Dolor neuropático. Cátedra Extraordinaria del Dolor
"Fundación Grünenthal" de la Universidad de Salamanca.
12. Cannabis y Cannabinoides en el tratamiento del dolor neuropático. Durán M, Capellá D: Cannabis y Cannabinoides en el tratamiento del dolor neuropático. DOLOR 2000; 20.
13. Recomendaciones para el tratamiento del dolor neuropático. González - Escalada, JR et al.: Recomendaciones para el tratamiento del dolor neuropático. Rev. Soc. Esp. Dolor[online]. 2009; 16 (8) 445-467.
14. Estimulación magnética transcraneal. Pascual- Leone A, Tormos- Muñoz JM: Estimulación magnética transcraneal: fundamentos y potencial de la modulación de redes neurales específicas. REV NEUROL 2008; 46 (1): S3-S10
15. Técnicas no invasivas de estimulación cerebral para el dolor crónico. O' Connel N et al: Non-invasive brain stimulation techniques for chronic pain (review). Cochrane Library (2011)
Agradecimientos
 |




Otro artículo magnífico y las imágenes que has elegido alucinantes. Estás haciendo un trabajo magnífico!!!
ResponderEliminarTodo esfuerzo merece la pena con comentarios como los tuyos! Gracias!!!
EliminarMuy bien explicado. Ahra mismo aprobaba un examen sobre dolor neuropático. Mañana no sé... Y con traductora oficial! Qué nivel! :P Las imágenes muy bien elegidas. Me duele todo ahora ;)
ResponderEliminarSí, es mejor pedir ayuda a profesionales por si me cuelo al traducir, y Almudena es una experta colaboradora :) Me alegro de que resulte claro. Muchas gracias! ;)
Eliminar